

呼吸器グループ
近年、我が国における肺癌患者数は人口の高齢化とともに著しい増加を示し、1998年、男性の肺癌死亡数は胃癌を抜いて癌部位別死亡のトップとなりました。人口10万人当たりの死亡数(粗死亡率)も依然として増加しています。年齢で調整した死亡率(年齢調整死亡率)は1990年頃より低下傾向に転じていますが、年齢調整した肺癌になる確率(年齢調整罹患率)は男女ともに増加しており、2015年には年間147,000人が罹患、120,000人が死亡すると予測されています。肺癌はますます重要な疾患となるでしょう。
ここではまず、一般的な肺癌の診療、とくに外科治療について概説し、その後で岡山大学呼吸器外科で行っている外科治療について解説します。
肺癌の主な発生原因はたばこで、肺癌患者の80~85%が喫煙者です。喫煙者が肺癌になる確率は非喫煙者の10~20倍で、喫煙開始年齢が若いほど、喫煙量が多いほど肺癌罹患率が高くなります。禁煙すると肺癌罹患リスクが喫煙継続者と比較して低下します。自分ではたばこを吸わない人でも周りに喫煙者がいると、点火部から立ち昇る煙を吸ってしまいます。これを受動喫煙といいます。受動喫煙者は非受動喫煙者と比較して肺癌罹患危険率が21~26%増加します。
JT全国喫煙者率調査では、我が国の男性の喫煙率は昭和40年頃がピークで83.7%と高かったのですが、その後は減少を続け平成21年では38.9%まで低下しました。一方、女性の喫煙率はほぼ横ばいの状態で平成21年度11.9%でした。(図1)。禁煙後5-10年以内に肺癌のリスクが喫煙継続者に比べて明らかに低下することから、肺癌予防のためには禁煙がとても重要です。
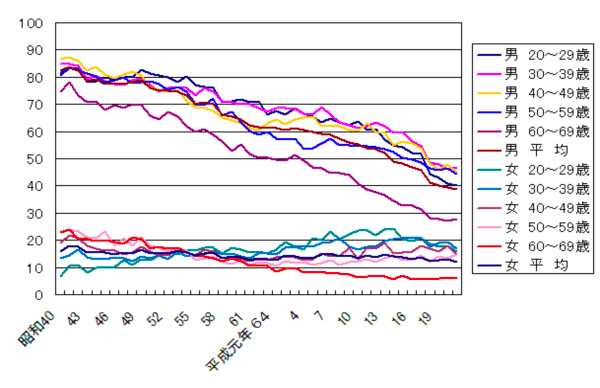
図1 JT全国喫煙者率調査のホームページより
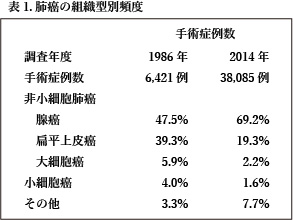
肺癌の組織型は、治療方針の違いから非小細胞癌と小細胞癌に大別されます。その頻度は手術例では腺癌、扁平上皮癌、大細胞癌、小細胞癌の順に多く、非手術例では腺癌、扁平上皮癌、小細胞癌、大細胞癌の順です。
日本胸部外科学会の手術統計(表1)では肺癌手術総数は30年間で約6倍に増加しました。内訳は、腺癌が3,050例から26,355例へ約8.5倍と大幅に増加しているのに対して、扁平上皮癌は2,525例から7,350例で約3倍の増加です。肺癌手術総数の増加は腺癌の増加によるものです。
発見動機とは肺癌患者が医療機関を初めて受診するきっかけになった原因のことで、ここから肺癌診療がスタートします。症状、他疾患観察中、検診(健診)などが挙げられます。
1)肺癌の臨床症状
主な症状は咳嗽、喀痰、血痰、発熱、呼吸困難、胸痛などです。これらの症状は扁平上皮癌を代表とする肺門型肺癌に特徴的です。肺野型肺癌では無症状のことが多く、他疾患観察中や検診で撮った胸部X線写真、胸部CTで発見されます。最近、多く見つかっているのは肺野型の肺腺癌です。
2)肺癌検診
胸部X線写真と喀痰細胞診を用いた肺癌集団検診により早期肺癌の発見比率は向上しますが、死亡抑制に対する効果は現時点では検診を行うよう勧めるだけの根拠が明確ではありません。しかし、最近ヘリカルCTを用いた肺癌検診は死亡率の低下につながるとの報告が出されました。検診で見つかる肺癌は早期発見、早期治療につながるため、お勧めします。
血液検査でチェックできる肺癌の腫瘍マーカーとしては、非小細胞肺癌ではCYFRA21-1, CEA, SLX, CA19-9, CA125, SCC, TPAなどがあります。小細胞肺癌に特異的なマーカーとしてはNSE,ProGRPがあります。検出感度はいずれも50%程度ですが、有意に上昇している場合は経過の評価や治療効果判定に有用です。
2)画像による肺癌の検出
胸部X線写真は簡便で広く普及した検査方法であり、肺癌検出のために強く勧められます。また、胸部X線写真で異常がある時は胸部CT検査が強く勧められます。
胸部X線写真による肺癌の検出感度は80%程度と報告されています。鎖骨と第一肋骨の交差する部位、心臓や横隔膜の後方では見逃しやすいので、胸部X写真だけでは安心はできません。また、肺胞置換型発育をする小型腺癌では病変が小さく淡いので検出率はわずか23%です。肺癌を検出する方法として胸部CTは最も有効な方法で、特に前述の肺胞置換型発育をする小型腺癌はスリガラス陰影(ground glass opacity:GGO)を呈し、CTでのみ発見されます。
肺癌の質的診断として高分解能CT、造影CT、MRI、PET、およびこれらの画像の経時的比較などの方法が推奨されています。
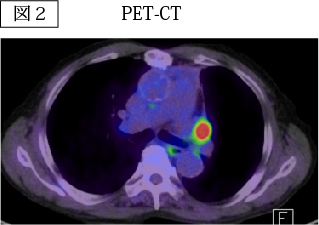
FDG-PET検査はブドウ糖類似の放射性薬剤FDGを静注し、20-30分後よりPETカメラで体の各組織から届いたRIの強さを直接画像にするものです。通常では集積の認められない部位に集積が認められれば陽性と判断します。FDGは増殖速度の速い細胞に多く取り込まれることから、FDG-PETを用いることにより良性悪性の診断率が向上しました。Standard uptake value (SUV) は半定量的指標ですが、良性悪性の評価や悪性度の強さの評価に参考となります。図2.は肺癌患者さんのPET-CTです。左肺門に腫瘤陰影に一致してFDGの集積(赤い部分)が認められます。組織診断では扁平上皮癌でした。
肺癌治療を行う前には組織診断、細胞診断で確定診断を行うことが強く勧められています。方法は、喀痰細胞診、気管支鏡による生検、CT下針生検、胸腔鏡下生検、開胸生検などがあります。
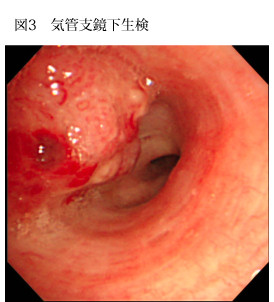
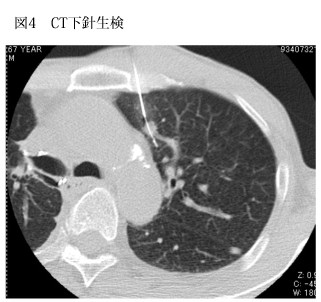
喀痰細胞診は簡便、非侵襲的で肺門部肺癌には有用ですが、肺野型肺癌の検出率は低くなります。気管支鏡下生検は図3のような肺門型肺癌には有効で、強く勧められます。肺野型病変に対しては、透視により描出できるかどうか、病変の大きさ、術者の技術などにより適応を決定する必要があります。 CT下針生検は気管支鏡下生検ができないような淡い小結節(図4)に有用です。しかし、合併症として気胸の発生、まれではありますが播種や空気塞栓を起こすことがあり、慎重な対応が要求されます。
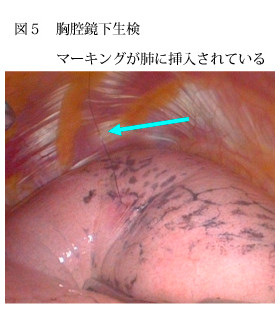
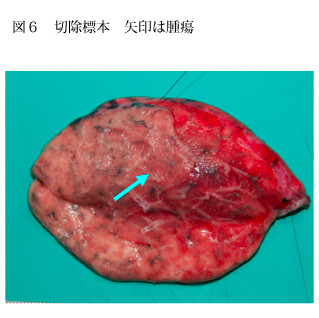
胸腔鏡下生検は腫瘍陰影(GGO)の近くにマーキングを入れて、肺部分切除を行います。病理診断の結果は肺腺癌でした。
肺癌と確定診断がつけば次にどこまで進行しているか調べることが必要となります。肺癌の転移が多い臓器としては肺、肝、副腎、脳、骨などが挙げられます。肺、肝、副腎の転移は原発巣診断のための胸部CT(造影)で同時に診断が可能です。脳転移は造影CTや造影MRIで、骨転移は骨シンチで診断されます。最近では、全身FDG-PETで、脳以外の遠隔転移を診断することが多くなってきました。
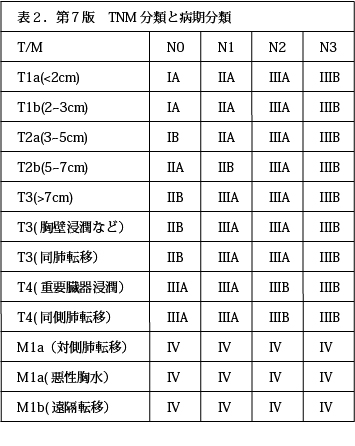
肺癌の進行度を表す方法として世界共通のTNM分類が用いられています。データをもとに改訂が行われ、現在のものは第7版です(表2)。また、TNM分類の中で共通の治療方針、同じような予後のものをグループ化したものが病期分類です。TNM分類のT因子は腫瘍のサイズ、浸潤を、N因子はリンパ節転移を、M因子は遠隔転移を意味しています。
肺癌の治療は臨床病期分類に基づいて概ね以下のように行われます。

癌の根治を目指した標準術式は、肺葉切除と縦隔リンパ節郭清術です。しかし、近年、肺癌検診の普及、診断技術の向上により小さな肺癌が多く見つかるようになり、この中で腫瘍径が2cm以下、リンパ節転移なしの早期肺癌に対して根治性を目指した積極的縮小手術としての区域切除が実施されるようになってきました。そして、その手術成績は標準術式である肺葉切除と比較して遜色ない結果が報告されました。一方、低侵襲手術として胸腔鏡下肺葉切除術の普及も著しいものがあります。しかし、この方法は胸壁への侵襲は多少軽度ですが、肺の切除容量は区域切除に比べて大きいものです。胸腔鏡を併用した小開胸での区域切除が理想的です。開胸手術も低侵襲化への工夫がされており、胸壁の筋肉(広背筋や前鋸筋)を切断しない、側方切開、腋窩前方切開などの筋肉温存小開胸法が用いられています。進行度に合わせた、安全で根治性を担保できる術式の選択が大切です。
術前に縦隔リンパ節に転移があると診断された場合(TNM分類でN2といいます)には、術前に化学療法(抗癌剤の投与)や化学放射線同時併用療法を行った後に手術を行う方法が採用されます。
肺尖部浸潤肺癌(肺の最上部から胸壁へ浸潤する肺癌でパンコースト型肺癌と呼びます)、気管分岐部、上大静脈、左心房、大動脈など重要臓器への浸潤を伴っている局所進行肺癌に対しては、化学放射線同時併用療法を行った後、拡大合併切除が行われます。椎骨の合併切除は整形外科と、左心房、大動脈の合併切除は心臓血管外科と共同で手術が行われます。しかし、このような拡大手術は高度な技術と設備が必要なことから、出来る施設は限られています。
肺癌の術後には、肺炎、呼吸不全など呼吸器系の合併症、心筋梗塞や不整脈など循環器系の合併症、脳出血、脳梗塞など脳神経系の合併症など、様々な合併症が発生します。これら術後合併症によって死亡された時の死亡率を、手術後30日以内の死亡率(30日死亡率)と退院することなく死亡する率(院内死亡率)で表現します。2008年全国で行われた肺癌症例27,885例の30日死亡率は0.4%、院内死亡率は0.9%でした。もちろん、手術前の患者さんの状態(年齢、合併症の有無、肺癌の進行など)に違いがありますので一概にはいえませんが、欧米の代表的な病院での院内死亡率が約2%であることから、日本の死亡率が低いことがわかります。
2002年に我が国において手術が行われた非小細胞肺癌4,170例の5年生存率はIA:89.3%, IB:77.9%, IIA:65.4%, IIB: 66.9%, IIIA:45.9%, IIIB:38.6%, IV:48.4%でした。